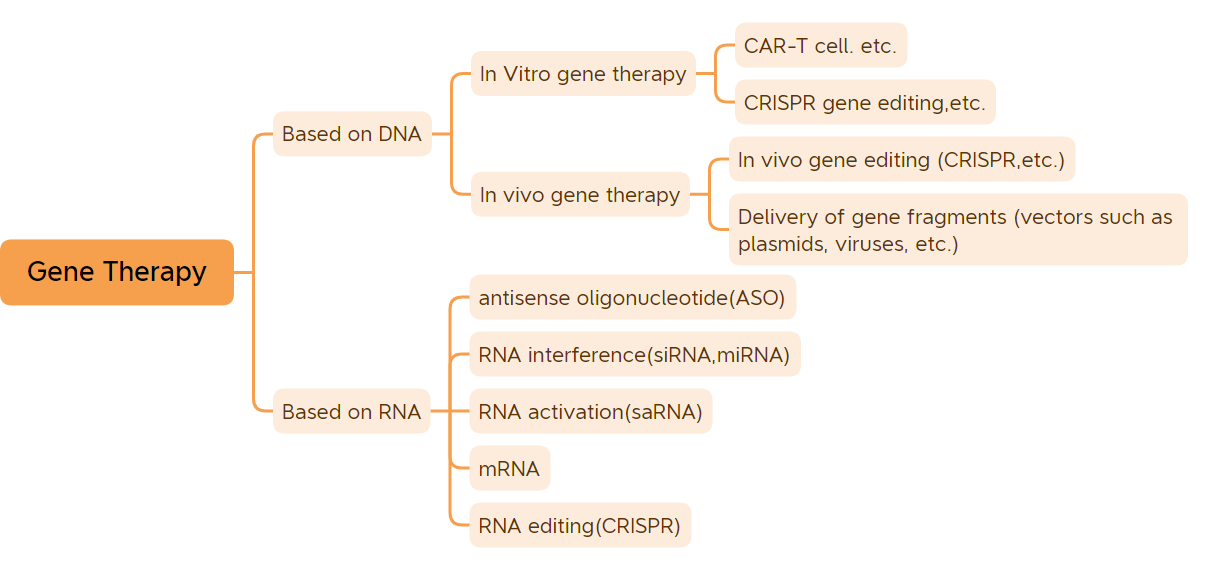
Is iad géinte na bunaonaid ghéiniteacha a rialaíonn tréithe.Seachas géinte roinnt víreas, atá comhdhéanta de RNA, tá géinte formhór na n-orgánach comhdhéanta de DNA.Is é an t-idirghníomhú idir géinte agus an comhshaol is cúis le formhór na ngalar orgánach.Is féidir le teiripe géin go bunúsach go leor galair a leigheas nó a mhaolú.Meastar gur réabhlóid i réimse na míochaine agus na cógaisíochta é géinteiripe.Áirítear le drugaí géinteiripe sa chiall leathan atá bunaithe ar dhrugaí DNA modhnaithe DNA (cosúil le drugaí géinteiripe in vivo bunaithe ar veicteoirí víreasacha, drugaí géinteiripe in vitro, drugaí plasmid naked, etc.) agus drugaí RNA (cosúil le drugaí oligonucleotide antisense, drugaí siRNA, agus géinteiripe mRNA, etc.);Cuimsíonn drugaí géinteiripe den chuid is mó drugaí plasmid DNA, drugaí géinteiripe bunaithe ar veicteoirí víreasacha, drugaí géinteiripe bunaithe ar veicteoirí baictéaracha, córais eagarthóireachta géine, agus drugaí teiripe cille le haghaidh modhnú géine in vitro.Tar éis blianta d'fhorbairt tortuous, tá torthaí cliniciúla spreagúla bainte amach ag drugaí géinteiripe.(Gan vacsaíní DNA agus vacsaíní mRNA a chomhaireamh) Faoi láthair, tá 45 druga géinteiripe ceadaithe le haghaidh margaíochta ar fud an domhain.Tá iomlán de 9 teiripí géine ceadaithe le haghaidh margaíochta i mbliana, lena n-áirítear 7 teiripí géine ceadaithe le haghaidh margaíochta den chéad uair i mbliana, is iad sin: CARVYKTI, Amvuttra, Upstaza, Roctavian, Hemgenix, Adsiladrin agus Ebvallo, (Nóta: Faomhadh an dá cheann eile sna Stáit Aontaithe i mbliana. An chéad bhaisc de teiripí géine ceadaithe le haghaidh margaíochta na Stát Aontaithe: ① a bhí formheasta ag an FDA teiripí géine margaíocht na Stáit Aontaithe: ① a bhí formheasta ag an FDA do mhargaíocht na Stáit Aontaithe: Lúnasa 2022, agus d’fhormheas an tAontas Eorpach é le haghaidh margaíochta in 2019; .) Le seoladh níos mó agus níos mó táirgí géinteiripe agus forbairt go mear ar theicneolaíocht géinteiripe, tá géinteiripe ar tí tréimhse mearfhorbartha a thabhairt isteach.
Aicmiú géinteiripe (Foinse íomhá: Bith-Mhaitrís)
Liostaíonn an t-alt seo 45 teiripí géine (gan vacsaíní DNA agus vacsaíní mRNA san áireamh) atá ceadaithe le haghaidh margaíochta.
1. Géinteiripe in vitro
(1) Strimvelis
Cuideachta: Arna fhorbairt ag GlaxoSmithKline (GSK).
Am chun an mhargaidh: D’fhaomh an tAontas Eorpach é le haghaidh margaíochta i mBealtaine 2016.
Tásca: Chun cóireáil a dhéanamh ar dhroch-easpa imdhíonachta comhcheangailte (SCID).
Nótaí: Is é próiseas ginearálta na teiripe seo ná gaschealla hematopoietic an othair féin a fháil ar dtús, iad a leathnú agus a chothú in vitro, ansin retrovirus a úsáid chun cóip géine ADA (adenosine deaminase) feidhmiúil a thabhairt isteach sna gaschealla hematopoietic, agus ar deireadh instealladh na gaschealla hematopoietic modhnaithe a ath-insileadh ar ais isteach sa chorp.Léiríonn torthaí cliniciúla gurb é an ráta marthanais 3 bliana d’othair ADA-SCID cóireáilte le Strimvelis ná 100%.
(2) Zalmoxis
Cuideachta: Arna léiriú ag an Iodáil MolMed Company.
Am chun an mhargaidh: Fuarthas údarú margaíochta coinníollach ón Aontas Eorpach in 2016.
Tásca: Úsáidtear é le haghaidh teiripe aidiúvach ar chóras imdhíonachta othar tar éis trasphlandú gascheall hematopoietic.
Nótaí: Is éard atá i Zalmoxis ná imdhíonteiripe géine féinmharaithe T allogeneic-chealla arna mhodhnú ag veicteoirí retroviral.Úsáideann an modh seo veicteoirí retroviral chun cealla T allogeneic a mhodhnú go géiniteach, ionas go gcuireann na cealla T géinmhodhnaithe géinte féinmharaithe 1NGFR agus HSV-TK Mut2 ar chumas daoine úsáid a bhaint as drugaí ganciclovir (ganciclovir) ag am ar bith chun cealla T a mharú a chuireann frithghníomhartha díobhálacha imdhíonachta orthu, cosc a chur ar mheath breise GVHD, agus atógáil feidhm imdhíonachta iar-oibriúcháin a chur ar fáil d'othair eslocoride eslocorttical ESCT.
(3) Invossa-K
Cuideachta: Arna fhorbairt ag TissueGene (KolonTissueGene).
Am chun an mhargaidh: Faofa le haghaidh liostú sa Chóiré Theas i mí Iúil 2017.
Tásca: Chun cóireáil airtríteas glúine degenerative.
Nótaí: Is géinteiripe cealla allogeneic é Invossa-K a bhaineann le chondrocítí daonna.Déantar na cealla allogeneic a mhodhnú go géiniteach in vitro, agus is féidir leis na cealla modhnaithe fachtóir fáis claochlaithe β1 (TGF-β1) a chur in iúl agus a secrete tar éis instealladh in-articular.β1), rud a fheabhsaíonn airíonna osteoarthritis.Léiríonn torthaí cliniciúla gur féidir le Invossa-K feabhas suntasach a dhéanamh ar airtríteas glúine.Rinne Riarachán Bia agus Drugaí na Cóiré é a chúlghairm in 2019 toisc gur chuir an monaróir lipéad mícheart ar na comhábhair a úsáideadh.
(4) Zynteglo
Cuideachta: Bluebird bio a rinne taighde agus forbairt air.
Am chun an mhargaidh: Faofa ag an Aontas Eorpach le haghaidh margaíochta in 2019, agus faofa ag an FDA le haghaidh margaíochta sna Stáit Aontaithe i mí Lúnasa 2022.
Tásca: Chun cóireáil a dhéanamh ar β-thalassemia atá ag brath ar fhuilaistriú.
Nótaí: Is éard atá i Zynteglo ná géinteiripe lentiviral in vitro a thugann isteach cóip fheidhmiúil den ghnáthghéine β-globin (géine βA-T87Q-globin) i gaschealla hematopoietic a thógtar ón othar trí veicteoir lentiviral, agus ansin athinstear na gaschealla hematopoietic uathathraithe uathlógacha seo isteach san othar.Nuair a bhíonn géine βA-T87Q-globin gnáth ag an othar, féadfaidh siad gnáth-phróitéin HbAT87Q a tháirgeadh, rud a d'fhéadfadh an gá atá le fuilaistriú a laghdú nó a dhíchur go héifeachtach.Teiripe aonuaire is ea é atá deartha chun fuilaistriúcháin ar feadh an tsaoil agus cógais ar feadh an tsaoil a athsholáthar d’othair atá 12 bhliain d’aois agus níos sine.
(5) Skysona
Cuideachta: Bluebird bio a rinne taighde agus forbairt air.
Am chun an mhargaidh: Faofa ag an Aontas Eorpach le haghaidh margaíochta i mí Iúil 2021, agus ceadaithe ag an FDA le haghaidh margaíochta sna Stáit Aontaithe i Meán Fómhair 2022.
Tásca: Le haghaidh cóireáil luath adrenoleukodystrophy cheirbreach (CALD).
Nótaí: Is é géinteiripe Skysona an t-aon ghéinteiripe aonuaire amháin atá ceadaithe chun cóireáil a dhéanamh ar adrenoleukodystrophy cheirbreach (CALD).Is éard atá i Skysona (elivaldogene autotemcel, Lenti-D) gascheall hematopoietic lentiviral in vitro géinteiripe Lenti-D.Is é seo a leanas nós imeachta ginearálta na teiripe: baintear gaschealla hematopoietic uathlógacha as an othar, aistrítear iad agus modhnaítear iad le lentivirus a iompraíonn an ghéin in vitro ABCD1 daonna, agus ansin ath-insileadh ar ais chuig an othar.Úsáidtear é chun cóireáil a dhéanamh ar othair faoi bhun 18 mbliana d’aois, ag iompar sócháin ghéine ABCD1, agus CALD.
(6) Cimriah
CUIDEACHTA: Arna fhorbairt ag Novartis.
Am chun an mhargaidh: Faofa ag an FDA le haghaidh margaíochta i mí Lúnasa 2017.
Tásca: Cóireáil leoicéime ghéarmhíochaine B-chill réamhtheachtaithe (GACH) agus DLBCL athiompaithe agus teasfhulangacha.
Nótaí: Is druga géinteiripe lentiviral in vitro é Kymriah, an chéad teiripe CAR-T a formheasadh le haghaidh margaíochta ar domhan, ag díriú ar CD19, agus ag baint úsáide as fachtóir comh-spreagthach 4-1BB.Tá sé ar phraghas $475,000 i SAM agus $313,000 sa tSeapáin.
(7) Seacarta
Cuideachta: Arna fhorbairt ag Kite Pharma, fochuideachta de chuid Gilead (GILD).
Am chun an mhargaidh: Faofa ag an FDA le haghaidh margaíochta i mí Dheireadh Fómhair 2017;Thug Fosun Kite teicneolaíocht Yescarta isteach ó Kite Pharma agus tháirgtear sa tSín é tar éis údarú a fháil.Faofa le haghaidh liostála sa tír.
Tásca: Chun liomfóma B-chealla mór athiompaithe nó teasfhulangacha a chóireáil.
Nótaí: Is géinteiripe retroviral in vitro é Yescarta, an dara teiripe CAR-T ceadaithe ar domhan.Díríonn sé ar CD19 agus glacann sé an cost-iomaitheoir CD28.Tá sé ar phraghas $373,000 sna Stáit Aontaithe.
(8) Tecartus
Cuideachta: Arna fhorbairt ag Gilead (GILD).
Am chun an mhargaidh: Faofa ag an FDA le haghaidh margaíochta i mí Iúil 2020.
Tásca: Le haghaidh liomfóma cille maintlín athiompaithe nó teasfhulangacha.
Nótaí: Is teiripe cille uathlógach CAR-T é Tecartus a dhíríonn ar CD19, agus is é an tríú teiripe CAR-T atá ceadaithe le haghaidh margaíochta ar domhan.
(9) Breyanzi
CUIDEACHTA: Arna fhorbairt ag Bristol-Myers Squibb (BMS).
Am chun an mhargaidh: Faofa ag an FDA le haghaidh margaíochta i mí Feabhra 2021.
Tásca: Liomfóma mór B-chealla (LBCL) athiompaithe nó teasfhulangacha (T/T).
Nótaí: Is géinteiripe in vitro é Breyanzi atá bunaithe ar an lentivirus, an ceathrú teiripe CAR-T atá ceadaithe le haghaidh margaíochta ar fud an domhain, ag díriú ar CD19.Is cloch mhíle é ceadú Breyanzi do Bristol-Myers Squibb i réimse na himdhíonteiripe ceallacha, a ghnóthaigh sé nuair a ghnóthaigh sé Celgene ar $74 billiún in 2019.
(10) Abecma
Cuideachta: Comhfhorbartha ag Bristol-Myers Squibb (BMS) agus bluebird bio.
Am chun an mhargaidh: Faofa ag an FDA le haghaidh margaíochta i mí an Mhárta 2021.
Tásca: miólóma iolrach athiompaithe nó teasfhulangach.
Nótaí: Is géinteiripe in vitro é Abecma atá bunaithe ar lentivirus, an chéad teiripe cille CAR-T ar domhan a dhíríonn ar BCMA, agus an cúigiú teiripe CAR-T arna fhaomhadh ag FDA.Is é prionsabal an druga ná gabhdóirí BCMA chimeric a chur in iúl ar chealla T an othair féin trí mhodhnú géine trí mheán lentivirus in vitro.Cóireáil chun deireadh a chur le cealla T neamh-ghéinmhodhnaithe in othair, agus ansin cealla T leasaithe a ath-iniúchadh, a lorgaíonn agus a mharaíonn cealla ailse a chuireann BCMA in iúl in othair.
(11) Libmeldy
CUIDEACHTA: Arna fhorbairt ag Orchard Therapeutics.
Am chun an mhargaidh: Faofa ag an Aontas Eorpach lena liostú i mí na Nollag 2020.
Tásca: Le haghaidh cóireáil leocodystrophy meitecromatach (MLD).
Nótaí: Is géinteiripe é Libmeldy atá bunaithe ar chealla CD34+ uathlógacha atá géinmhodhnaithe in vitro ag lentivirus.Léiríonn sonraí cliniciúla gur féidir le hinsileadh infhéitheach amháin de Libmeldy cúrsa MLD luath-thosaithe a athrú go héifeachtach i gcomparáid le lagú mótair agus cognaíocha trom in othair den aois chéanna gan chóireáil.
(12) Benoda
Cuideachta: Arna fhorbairt ag WuXi Giant Nuo.
Am chun an mhargaidh: Faofa go hoifigiúil ag NMPA i Meán Fómhair 2021.
Tásca: Cóireáil othair aosach le liomfóma B-chealla mór athiompaithe nó teasfhulangacha (r/r LBCL) tar éis teiripe shistéamach dara líne nó os a chionn.
Nótaí: Is géinteiripe frith-CD19 CAR-T é Beinoda, agus is é croí-tháirge WuXi Juro Company é freisin.Is é an dara táirge CAR-T atá ceadaithe sa tSín, ach amháin i gcás limfeach B-chealla mór athiompaithe/teasfhulangacha Tá sé beartaithe ag WuXi Giant Nuo instealladh Regiorensai a fhorbairt chun cóireáil a dhéanamh ar iliomad tásca eile, lena n-áirítear liomfóma follicular (FL), liomfóma mantle cille (MCL), leoicéime limficíteach ainsealach (CLL), leoicéime lymphocytic ainsealach (CLL), leoicéime B-chealla mór idirleata (limféime dara líne idirleata).
(13) CARVYKTI
Cuideachta: An chéad táirge de chuid Legend Biotech ceadaithe le haghaidh margaíochta.
Am chun an mhargaidh: Faofa ag an FDA le haghaidh margaíochta i mí Feabhra 2022.
Tásca: chun cóireáil a dhéanamh ar mhiolóma iolrach athiompaithe nó teasfhulangach (R/R MM).
Nótaí: Is géinteiripe imdhíonachta cille CAR-T é CARVYKTI (ciltacabtagene autoleucel, Cilta-cel) ina bhfuil dhá antasubstaint aon-fhearainn a dhíríonn ar antaigin aibithe B-chealla (BCMA).Léiríonn sonraí go bhfuil CARVYKTI In othair le mialóma iolrach athiompaithe nó teasfhulangacha a fuair ceithre theiripe roimh ré nó níos mó (lena n-áirítear coscairí proteasome, inmunomodulators agus antasubstaintí monachlónacha frith-CD38), tá ráta freagartha foriomlán de 98%.
(14)Éabhall
CUIDEACHTA: Arna fhorbairt ag Atara Biotherapeutics.
an Coimisiún Eorpach (CE) le haghaidh margaíochta i mí na Nollag 2022 , is é an chéad teiripe T chealla T uilíoch ar domhan a formheasadh le haghaidh margaíochta.
Tásca: Mar mhonaiteiripe do ghalar lymphoproliferative iar-trasphlandúcháin (EBV+PTLD) a bhaineann le víreas Epstein-Barr (EBV), ní mór go mbeadh na hothair a fhaigheann cóireáil ina ndaoine fásta agus ina leanaí os cionn 2 bhliain d'aois a fuair teiripe drugaí amháin eile ar a laghad roimhe seo.
Nótaí: Is géinteiripe uilíoch T-chealla uile-ghinéineach é Ebvallo a dhíríonn ar chealla ionfhabhtaithe EBV agus a dhíchuireann ar bhealach atá srianta le HLA.Tá ceadú na teiripe seo bunaithe ar thorthaí staidéar trialach cliniciúla céim 3 ríthábhachtach, agus léirigh na torthaí go raibh ORR an ghrúpa HCT agus an ghrúpa SOT 50%.Ba é an ráta loghadh iomlán (CR) 26.3%, ba é an ráta loghadh páirteach (PR) 23.7%, agus ba é an t-am airmheánach chun loghadh (TTR) ná 1.1 mí.As na 19 othar a bhain loghadh amach, bhí ré freagartha (DOR) de níos mó ná 6 mhí ag 11 acu.Ina theannta sin, i dtéarmaí sábháilteachta, níor tharla aon fhrithghníomhartha díobhálacha cosúil le galar graft-versus-host (GvHD) nó siondróm scaoileadh cytokine a bhaineann le Ebvallo.
2. Géinteiripe in vivo bunaithe ar veicteoirí víreasacha
(1) Inscne/Jin Sheng
Cuideachta: Arna fhorbairt ag Shenzhen Saibainuo Company.
Am chun an mhargaidh: Ceadaithe le bheith liostaithe sa tSín i 2003.
Tásca: Chun carcinoma cille squamous ceann agus muineál a chóireáil.
Nóta: Instealladh athchuingreach adenovirus p53 daonna Is druga géinteiripe veicteoir adenovirus é Gendicine/Jinyousheng a bhfuil cearta maoine intleachtúla neamhspleácha faoi úinéireacht Shenzhen Saibainuo Company aige.Tá adenovirus cineál daonna 5 comhdhéanta de adenovirus daonna cineál 5. Is é an chéad cheann an príomh-struchtúr d'éifeacht frith-meall an druga, agus gníomhaíonn an dara ceann den chuid is mó mar iompróir.Iompraíonn an veicteoir adenovirus an ghéin theiripeach p53 isteach sa spriocchill, cuireann sé an géine suppressor meall p53 in iúl sa spriocchill, agus a léiriú géine Is féidir leis an táirge éagsúlacht géinte frith-ailse a rialáil agus gníomhaíochtaí éagsúla oncogenes a rialáil, rud a fheabhsaíonn éifeacht suppressor meall an chomhlachta agus an cuspóir a bhaint amach chun siadaí a mharú.
(2) Rigvir
Cuideachta: Arna fhorbairt ag Latima Company, an Laitvia.
Am liostála: Faofa le haghaidh liostú sa Laitvia i 2004.
Tásca: Chun melanoma a chóireáil.
Nótaí: Is géinteiripe é Rigvir atá bunaithe ar veicteoir eintreachivíreas géinmhodhnaithe ECHO-7.Faoi láthair, tá an druga glactha sa Laitvia, san Eastóin, sa Pholainn, san Airméin, sa Bhealarúis, etc., agus tá sé faoi chlárú EMA i dtíortha an AE freisin.Tá cásanna cliniciúla le deich mbliana anuas cruthaithe go bhfuil víreas oncolytic Rigvir sábháilte agus éifeachtach, agus féadann sé ráta marthanais othair melanoma a mhéadú 4-6 huaire.Ina theannta sin, tá an teiripe seo infheidhme freisin maidir le héagsúlacht ailsí eile, lena n-áirítear ailse cholaireicteach, ailse pancreatach, ailse bladder Ailse, ailse duáin, ailse próstatach, ailse scamhóg, ailse útarach, lymphosarcoma, etc.
(3) Oncorine
Cuideachta: Arna fhorbairt ag Shanghai Sanwei Biological Company.
Am chun an mhargaidh: Ceadaithe le bheith liostaithe sa tSín i 2005.
Tásca: cóireáil siadaí ceann agus muineál, ailse ae, ailse pancreatic, ailse cheirbheacsach agus ailsí eile.
Nótaí: Is táirge géinteiripe víreas oncolytic é Oncorine (安科瑞) a úsáideann adenovirus mar iompróir.Faightear adenovirus oncolytic, ar féidir é a mhacasamhlú go sonrach i siadaí géine easnamhach nó neamhghnácha p53, as a dtiocfaidh lysis cealla meall, rud a mharaíonn cealla meall.gan damáiste a dhéanamh do chealla gnáth.Tá sé léirithe ag staidéir chliniciúla go bhfuil sábháilteacht agus éifeachtúlacht mhaith ag Ankerui d'éagsúlacht siadaí urchóideacha.
(4) Glybera
Cuideachta: Arna fhorbairt ag uniQure.
Am chun an mhargaidh: Faofa le haghaidh liostú san Eoraip in 2012.
Tásca: Déileáil le heasnamh lipoprotein lipáis (LPLD) le eipeasóid tromchúiseacha nó athfhillteacha pancreatitis in ainneoin aiste bia saille srianta.
Nótaí: Is druga géinteiripe é Glybera (alipoprotein tiparvovec) atá bunaithe ar AAV, a úsáideann AAV mar iompróir chun an ghéine teiripeach LPL a aistriú isteach i gcealla muscle, ionas gur féidir leis na cealla comhfhreagracha méid áirithe de lipoprotein lipase a tháirgeadh, chun an galar a mhaolú, tá an teiripe seo éifeachtach ar feadh i bhfad (is féidir éifeacht an druga a riaradh uair amháin ar feadh blianta fada).Tarraingíodh siar an druga ón margadh i 2017. D'fhéadfadh go mbeadh baint ag an gcúis lena tharraingt siar le dhá fhachtóir: ardphraghas agus éileamh teoranta an mhargaidh.Tá meánchostas cóireála an druga chomh hard le US$1 milliún, agus níl ach othar amháin tar éis é a cheannach agus a úsáid go dtí seo.Cé go bhfuil US$900,000 aisíoctha ag an gcomhlacht árachais leighis as, is ualach measartha mór é don chuideachta árachais freisin.Ina theannta sin, tá na tásca ar a ndírítear leis an druga ró-annamh, le ráta minicíochta de thart ar 1 in 1 milliún agus ráta ard mídhiagnóis.
(5) Ilygic
Cuideachta: Arna fhorbairt ag Amgen.
Am chun an mhargaidh: In 2015, ceadaíodh é a liostú sna Stáit Aontaithe agus san Aontas Eorpach.
Tásca: Cóireáil loit meileanóma nach féidir a bhaint go hiomlán le máinliacht.
Nótaí: Is víreas herpes simplex maolaithe cineál 1 é Imlygic atá modhnaithe ag teicneolaíocht ghéiniteach (a chuid blúirí géine ICP34.5 agus ICP47 a scriosadh, agus géine GM-CSF fachtóir a spreagann coilíneacht granulocyte daonna a spreagann GM-CSF isteach sa víreas) (HSV-1) Is é víreas oncolytic an chéad theiripe víreas arna cheadú ag FDA.Is é an modh riaracháin instealladh intralesional, is féidir a instealladh go díreach isteach i loit melanoma chun réabfaidh cealla meall, scaoileadh antaiginí meall-díorthaithe agus GM-CSF, agus frith-meall freagraí imdhíonachta a chur chun cinn.
(6) Luxturna
Cuideachta: Arna fhorbairt ag Spark Therapeutics, fochuideachta de chuid Roche.
Am chun an mhargaidh: D’fhaomh an FDA é le haghaidh margaíochta in 2017, agus ansin faomhadh é le haghaidh margaíochta san Eoraip in 2018.
Tásca: Chun cóireáil a dhéanamh ar leanaí agus ar dhaoine fásta a chaill radharc mar gheall ar shócháin géine RPE65 ar chóip dhúbailte ach a choinníonn líon leordhóthanach cealla reitineacha inmharthana.
Nótaí: Is éard atá i Luxturna ná géinteiripe bunaithe ar AAV a riartar trí instealladh subretinal.Úsáideann an ghéinteiripe AAV2 mar iompróir chun cóip fheidhmiúil den ghnáthghéine RPE65 a thabhairt isteach i gcealla reitineacha an othair, ionas go gcuireann na cealla comhfhreagracha an gnáthphróitéin RPE65 in iúl, ag déanamh suas d'easnamh próitéine RPE65 an othair, rud a fheabhsú fís an othair.
(7) Zolgensma
Cuideachta: Arna fhorbairt ag AveXis, fochuideachta de chuid Novartis.
Am chun an mhargaidh: Faofa ag an FDA le haghaidh margaíochta i mBealtaine 2019.
Tásca: Cóireáil Atrophy Mhatánach Dhromlaigh (SMA) othair faoi 2 bhliain d'aois.
Nótaí: Is géinteiripe é Zolgensma atá bunaithe ar veicteoir AAV.Is é an druga seo an t-aon phlean cóireála aonuaire le haghaidh atrophy matáin dhromlaigh atá ceadaithe le haghaidh margaíochta ar fud an domhain.Osclaíonn seoladh an druga ré nua maidir le cóireáil atrophy mhatánach dhromlaigh.leathanach, is cloch mhíle dul chun cinn é.Úsáideann an ghéinteiripe seo veicteoir scAAV9 chun gnáthghéine SMN1 a thabhairt isteach san othar trí insileadh infhéitheach chun gnáthphróitéin SMN1 a tháirgeadh, rud a fheabhsaíonn feidhm na gceall a bhfuil tionchar acu ar nós néaróin mhótair.I gcodarsnacht leis sin, éilíonn na drugaí SMA Spinraza agus Evrysdi dáileoga fadtéarmacha arís agus arís eile.Tugtar Spinraza trí instealladh dromlaigh gach ceithre mhí, agus is druga laethúil ó bhéal é Evrysdi.
(8) Delytact
Cuideachta: Arna fhorbairt ag Daiichi Sankyo Company Limited (TYO: 4568).
Am chun an mhargaidh: Faomhadh coinníollach ó Aireacht Sláinte, Saothair agus Leasa na Seapáine (MHLW) i mí an Mheithimh 2021.
Tásca: Le haghaidh cóireáil glioma urchóideacha.
Nótaí: Is é Delytact an ceathrú táirge géinteiripe víreas oncolaíoch a formheasadh ar fud an domhain, agus an chéad táirge víreas oncolaíoch a formheasadh le haghaidh cóireáil glioma urchóideach.Is víreas oncolaíoch cineál 1 (HSV-1) víreas herpes simplex a ndearnadh innealtóireacht ghéiniteach air a d'fhorbair an Dr. Todo agus a chomhghleacaithe é Delytact.Tugann Delytact sócháin scriosta breise isteach sa genome G207 den dara glúin HSV-1, ag feabhsú a mhacasamhlú roghnach i gcealla ailse agus ionduchtú freagraí imdhíonachta frith-meall agus ard-sábháilteacht á chothabháil.Is é Delytact an chéad HSV-1 oncolytic tríú glúin atá faoi mheastóireacht chliniciúil faoi láthair.Tá formheas Delytact sa tSeapáin bunaithe go príomha ar thriail chliniciúil aon lámh amháin de chéim 2.In othair le glioblastoma athfhillteach, bhain Delytact críochphointe príomhúil an ráta marthanais aon bhliana amach, agus léirigh na torthaí gur léirigh Delytact éifeachtúlacht níos fearr i gcomparáid le G207.Fórsa macasamhail láidir agus gníomhaíocht antitumor níos airde.Bhí sé seo éifeachtach i múnlaí siadaí soladacha de chíche, próstatach, schwannomas, nasopharyngeal, hepatocellular, cholaireicteach, urchóideacha urchóideacha sheath nerve forimeallach, agus ailse thyroid.
(9) Upstaza
CUIDEACHTA: Arna fhorbairt ag PTC Therapeutics, Inc. (NASDAQ: PTCT).
Am chun an mhargaidh: Faofa ag an Aontas Eorpach le haghaidh margaíochta i mí Iúil 2022.
Tásca: Le haghaidh easnamh aramatacha L-aimínaigéad decarboxylase (AADC), tá sé ceadaithe chun cóireáil a dhéanamh ar othair atá 18 mí d'aois agus níos sine.
Nótaí: Is géinteiripe in vivo é Upstaza™ (eladocagene exuparvovec) a bhfuil víreas adeno-ghaolmhar de chineál 2 (AAV2) mar an t-iompróir.Éiríonn othair tinn de bharr sócháin sa ghéin a ionchódaíonn an einsím AADC.Tá géine sláintiúil ag AAV2 a ionchódaíonn an einsím AADC.Baineann an fhoirm cúitimh géine amach éifeacht theiripeach.Go teoiriciúil, tá riarachán amháin éifeachtach ar feadh i bhfad.Is é seo an chéad ghéinteiripe a mhargaítear a instealladh go díreach isteach san inchinn.Tá an t-údarú margaíochta infheidhme maidir le 27 mBallstát uile an AE, chomh maith leis an Íoslainn, an Iorua agus Lichtinstéin.
(10) Rotachtach
Cuideachta: Arna fhorbairt ag BioMarin Pharmaceutical (BioMarin).
Am chun an mhargaidh: Faofa le haghaidh margaíochta ag an Aontas Eorpach i mí Lúnasa 2022;údarú margaíochta ó Riarachán Leigheasra agus Táirgí Cúraim Sláinte na RA (MHRA) i mí na Samhna 2022.
Tásca: Chun cóireáil a dhéanamh ar othair aosacha a bhfuil hemophilia trom orthu nach bhfuil aon stair de chosc ar fhachtóirí FVIII acu agus atá diúltach d'antasubstaintí AAV5.
Nótaí: Úsáideann Roctavian (valoctocogene roxaparvovec) AAV5 mar veicteoir agus úsáideann sé an tionscnóir a bhaineann go sonrach leis an ae daonna HLP chun slonn fachtóir téachtadh daonna VIII (FVIII) a thiomáint agus scriostar an fearann B.Tá cinneadh an Choimisiúin Eorpaigh chun margaíocht valoctocogene roxaparvovec a fhormheas bunaithe ar shonraí foriomlána thionscadal forbartha cliniciúla an druga.Ina measc, léirigh torthaí na trialach cliniciúla céim III GENER8-1, i gcomparáid le sonraí na bliana roimh an gclárú, tar éis insileadh aonair de valoctocogene roxaparvovec, laghdaítear ráta fuilithe bliantúil an ábhair (ABR) go suntasach, laghdaítear minicíocht úsáide ullmhóidí próitéine fachtóir téachtadh athchuingreach VIII (F8), nó go laghdaítear gníomhaíocht fola i gcorp F8 go suntasach.Tar éis 4 seachtaine de chóireáil, laghdaíodh ráta úsáide bliantúil F8 an ábhair agus ABR a éilíonn cóireáil 99% agus 84%, faoi seach, agus bhí an difríocht suntasach go staitistiúil (p <0.001).Bhí an phróifíl sábháilteachta go maith, agus níor tuairiscíodh aon chosc ar fhachtóir F8, fo-iarmhairtí urchóideacha nó thrombóise, agus níor tuairiscíodh aon imeachtaí díobhálacha tromchúiseacha a bhain le cóireáil (SAEanna).
(11) Hemgenix
Cuideachta: Arna fhorbairt ag UniQure Corporation.
Am chun an mhargaidh: Faofa ag an FDA le haghaidh margaíochta i mí na Samhna 2022.
Tásca: Chun cóireáil a dhéanamh ar othair aosach le hemophilia B.
Nótaí: Is géinteiripe é Hemgenix atá bunaithe ar an veicteoir AAV5.Tá an druga feistithe leis an bhfachtóir téachtaithe IX (FIX) athraitheach géine FIX-Padua, a riartar go hinfhéitheach.Tar éis an riaracháin, is féidir leis an géine an fachtóir téachtadh FIX a chur in iúl san ae agus secrete Tar éis dul isteach san fhuil chun an fheidhm téachtadh a fheidhmiú, ionas go mbainfear amach an cuspóir cóireála, go teoiriciúil, tá riarachán amháin éifeachtach ar feadh i bhfad.
(12) Adstiladrin
Cuideachta: Arna fhorbairt ag Ferring Pharmaceuticals .
Am chun an mhargaidh: Faofa ag an FDA le haghaidh margaíochta i mí na Nollag 2022.
Tásca: Chun cóireáil a dhéanamh ar ailse lamhnán neamh-ionrach muscle ard-riosca (NMIBC) nach bhfreagraíonn do Bacillus Calmette-Guerin (BCG).
Nótaí: Is géinteiripe é Adsiladrin atá bunaithe ar veicteoir adenoviral neamh-mhacasamhlú, ar féidir leis próitéin interferon alfa-2b a ró-bhrú i gcealla sprice, agus a riartar trí chaitidéar fuail isteach sa lamhnán (arna riar uair amháin gach trí mhí), is féidir leis an veicteoir víreas ionfhabhtú a dhéanamh go héifeachtach isteach i gcealla bhalla an lamhnáin, agus ansin an éifeacht overexraplfa.Mar sin déanann an modh nua géinteiripe seo cealla balla lamhnán an othair féin a chlaochlú go “monarcha” miondúil a tháirgeann interferon, rud a chuireann le cumas an othair ailse a chomhrac.
Rinneadh measúnú ar shábháilteacht agus ar éifeachtúlacht Adstiladrin i staidéar cliniciúil ilionad lena n-áirítear 157 othar a raibh ardriosca BCG neamhfhreagrach NMIBC acu.Fuair othair Adsiladrin gach trí mhí ar feadh suas le 12 mhí, nó go dtí go raibh tocsaineacht do-ghlactha le cóireáil nó go dtarlaíonn sé arís ar ardghrád NMIBC.Tríd is tríd, d'éirigh le 51 faoin gcéad d'othair chláraithe a ndearnadh cóireáil orthu le Adsiladrin freagra iomlán a bhaint amach (imithe ar gach comhartha ailse a chonacthas ar chistoscopy, ar fhíochán bithóipse, agus ar fhual).
3. Drugaí beaga aigéid núicléacha
(1) Vitravene
Cuideachta: Comhfhorbartha ag Ionis Pharma (Isis Pharma roimhe seo) agus Novartis.
Am chun an mhargaidh: I 1998 agus 1999, cheadaigh FDA agus EMA an AE é le haghaidh margaíochta.
Tásca: Chun cóireáil retinitis cytomegalovirus in othair VEID-deimhneach.
Nótaí: Is druga antisense oligonucleotide é Vitravene, arb é an chéad druga oligonucleotide atá ceadaithe le haghaidh margaíochta ar domhan.Ag an gcéim tosaigh den liostú, bhí éileamh an mhargaidh ar dhrugaí frith-CMV an-phráinneach;níos déanaí, mar gheall ar fhorbairt teiripe antiretroviral an-ghníomhach, thit líon na gcásanna CMV go géar.Mar gheall ar éileamh an mhargaidh sluggish, seoladh an druga i 2002 agus 2006 Tarraingt siar i dtíortha an AE agus na Stáit Aontaithe.
(2) Macugen
Cuideachta: Comh-fhorbartha ag Pfizer agus Eyetech.
Am chun an mhargaidh: Faofa le haghaidh liostú sna Stáit Aontaithe i 2004.
Tásca: Chun cóireáil a dhéanamh ar dhíghiniúint macúlach neovascular a bhaineann le haois.
Nótaí: Is druga oligonucleotide modhnaithe pegylated é Macugen, ar féidir leis fachtóir fáis endothelial soithíoch (fochineál VEGF165) a dhíriú agus a cheangal, agus is é an modh riaracháin instealladh intravitreal.
(3) Defitelio
Cuideachta: Arna fhorbairt ag Jazz Pharmaceuticals.
Am chun an mhargaidh: D’fhaomh an tAontas Eorpach é le haghaidh margaíochta in 2013 agus d’fhaomh an FDA é le haghaidh margaíochta i Márta 2016.
Tásca: Chun cóireáil a dhéanamh ar ghalair hepatic veno-occlusive a bhaineann le mífheidhm duánach nó scamhógach tar éis trasphlandú gascheall hematopoietic.
Nótaí: Is druga oligonucleotide é Defitelio, ar meascán é d'oligonucleotides a bhfuil airíonna plasmin aige.Tarraingthe siar ón margadh in 2009 ar chúiseanna tráchtála.
(4) Cionamró
Cuideachta: Comh-fhorbartha ag Ionis Pharma agus Kastle.
Am chun an mhargaidh: In 2013, faomhadh é le haghaidh margaíochta sna Stáit Aontaithe mar dhruga dílleachta.
Tásca: Chun cóireáil aidiúvach ar hypercholesterolemia teaghlaigh homozygous.
Nótaí: Is druga oligonucleotide antisense é Kynamro, ar oligonucleotide antaisí é a dhíríonn ar apo B-100 mRNA daonna.Déantar Kynamro a riaradh mar 200 mg subcutaneously uair sa tseachtain.
(5) Spionra
Cuideachta: Arna fhorbairt ag Ionis Pharmaceuticals.
Am chun an mhargaidh: Faofa ag an FDA le haghaidh margaíochta i mí na Nollag 2016.
Tásca: Chun cóireáil atrophy mhatánach dhromlaigh (SMA).
Nótaí: Is druga oligonucleotide antisense é Spinraza (nusinersen).Trí cheangal a dhéanamh ar shuíomh scoilteachta SMN2 exon 7, is féidir le Spinraza scoilteacht RNA géine SMN2 a athrú, rud a mhéadaíonn táirgeadh próitéin SMN atá ag feidhmiú go hiomlán.I mí Lúnasa 2016, d’fheidhmigh BIOGEN a rogha chun na cearta domhanda chun Spinraza a fháil.Níor thosaigh Spinraza a chéad triail chliniciúil i ndaoine ach i 2011. I díreach 5 bliana, d'fhormheas an FDA é le haghaidh margaíochta i 2016, rud a léiríonn aitheantas iomlán an FDA ar a éifeachtúlacht.Ceadaíodh an druga le haghaidh margaíochta sa tSín i mí Aibreáin 2019. Bhí an timthriall ceadaithe iomlán do Spinraza sa tSín níos lú ná 6 mhí, agus bhí sé 2 bhliain agus 2 mhí ó faomhadh Spinraza ar dtús sna Stáit Aontaithe.Tá luas an liostála sa tSín an-tapa cheana féin.Tá sé seo mar gheall ar an bhfíric freisin gur eisigh an Lárionad um Mheasúnú Drugaí an “Fógra maidir le Foilsiú Liosta an Chéad Bhaisc de Dhrugaí Nua Thar Lear a bhfuil Teastáil go Práinneach i gCleachtas Cliniciúil” ar 1 Samhain, 2018, agus áiríodh é sa chéad bhaisc de 40 druga nua eachtrach le haghaidh athbhreithniú luathaithe, ina raibh Spinraza rangaithe.
(6) Exondys 51
Cuideachta: Arna fhorbairt ag AVI BioPharma (athainmníodh níos déanaí Sarepta Therapeutics).
Am chun an mhargaidh: I mí Mheán Fómhair 2016, cheadaigh an FDA é le haghaidh margaíochta.
Tásca: Chun diostróife mhatánach Duchenne (DMD) a chóireáil le exon 51 gan bacadh le sóchán géine sa ghéin DMD.
Nótaí: Is druga oligonucleotide antisense é Exondys 51, is féidir leis an oligonucleotide antisense ceangal a dhéanamh le seasamh exon 51 de réamh-mRNA de ghéine DMD, agus mar thoradh air sin foirmiú mRNA aibí, tá cuid de exon 51 bac ar Excision, rud a cheartú go páirteach ar an mRNA léamh frámaí, ag cabhrú le roinnt othar a fhoirmiú na próitéiní a ghiorrú an sintrófaithe, trí fhráma léitheoireachta a fheabhsú trí shintéisí. comharthaí.
(7) Tegsedi
Cuideachta: Arna fhorbairt ag Ionis Pharmaceuticals.
Am chun an mhargaidh: D’fhaomh an tAontas Eorpach é le haghaidh margaíochta i mí Iúil 2018.
Tásca: Chun cóireáil a dhéanamh ar amyloidosis transthyretin oidhreachtúil (hATTR).
Nótaí: Is druga oligonucleotide antisense é Tegsedi a dhíríonn ar mRNA trasthyretin.Is é an chéad druga atá ceadaithe ar domhan do chóireáil hATTR.Déantar é a riaradh trí instealladh subcutaneous.Laghdaíonn an druga táirgeadh próitéin ATTR trí dhíriú ar an mRNA de transthyretin (ATTR), agus tá cóimheas tairbhe-riosca maith aige i gcóireáil ATTR, agus tá neuropathy agus cáilíocht beatha an othair feabhsaithe go mór, agus tá sé ag luí le cineálacha sócháin TTR, Ní raibh céim an ghalair ná láithreacht cardiomyopathy ábhartha.
(8) Onpattro
Cuideachta: Comhfhorbartha ag Alnylam Corporation agus Sanofi Corporation.
Am chun an mhargaidh: Faofa le haghaidh liostú sna Stáit Aontaithe in 2018.
Tásca: Chun cóireáil a dhéanamh ar amyloidosis transthyretin oidhreachtúil (hATTR).
Nótaí: Is druga siRNA é Onpattro a dhíríonn ar mRNA transthyretin, a laghdaíonn táirgeadh próitéin ATTR san ae agus a laghdaíonn carnadh taiscí amyloid i nerves forimeallacha trí dhíriú ar an mRNA de transthyretin (ATTR), rud a fheabhsú agus a mhaolú comharthaí galair.
(9) Givlaari
Cuideachta: Arna fhorbairt ag Alnylam Corporation.
Am chun an mhargaidh: Faofa ag an FDA le haghaidh margaíochta i mí na Samhna 2019.
Tásca: Chun cóireáil a dhéanamh ar phorphyria hepatic géarmhíochaine (AHP) i ndaoine fásta.
Nótaí: Is druga siRNA é Givlaari, arb é an dara druga siRNA é a formheasadh le haghaidh margaíochta tar éis Onpattro.Is é an bealach riaracháin instealladh subcutaneous.Díríonn an druga an mRNA de phróitéin ALAS1, agus féadann cóireáil mhíosúil le Givlaari leibhéal ALAS1 san ae a laghdú go suntasach agus go buan, rud a laghdóidh leibhéil ALA agus PBG néara-tocsaineacha go dtí an gnáthraon, agus ar an mbealach sin comharthaí galair an othair a mhaolú.Léirigh na sonraí go raibh laghdú 74% ar líon na n-urghabhálacha ag othair a ndearnadh cóireáil orthu le Givlaari i gcomparáid leis an ngrúpa phlaicéabó.
(10) Vyondys53
CUIDEACHTA: Arna fhorbairt ag Sarepta Therapeutics.
Am chun an mhargaidh: Faofa ag an FDA le haghaidh margaíochta i mí na Nollag 2019.
Tásca: Chun cóireáil a dhéanamh ar othair DMD le géine dystrofin exon 53 splicing mutation.
Nótaí: Is druga antisense oligonucleotide é Vyondys 53, a dhíríonn ar phróiseas splicing na réamh-mRNA diostróifín.Tá Exon 53 teasctha go páirteach, ie níl sé i láthair ar an mRNA aibí, agus tá sé deartha chun diostróifín teasctha ach fós feidhmiúil a tháirgeadh, rud a chuireann feabhas ar chumas aclaíochta na n-othar.
(11) Bealachlivra
Cuideachta: Arna fhorbairt ag Ionis Pharmaceuticals agus a fhochuideachta Akcea Therapeutics.
Am chun an mhargaidh: D’fhormheas an Ghníomhaireacht Leigheasra Eorpach (EMA) é le haghaidh margaíochta i mBealtaine 2019.
Tásca: Mar theiripe aidiúvach chomh maith le rialú aiste bia in othair aosach a bhfuil siondróm chylomicronemia teaghlaigh (FCS) orthu.
Nótaí: Is druga oligonucleotide antisense é Waylivra, arb é an chéad druga atá ceadaithe le haghaidh margaíochta ar domhan le haghaidh cóireáil FCS.
(12) Leqvio
Cuideachta: Arna fhorbairt ag Novartis.
Am chun an mhargaidh: Faofa ag an Aontas Eorpach le haghaidh margaíochta i mí na Nollag 2020.
Tásca: Chun cóireáil a dhéanamh ar dhaoine fásta le hypercholesterolemia bunscoile (heitrisigeach teaghlaigh agus neamhtheaghlaigh) nó dyslipidemia measctha.
Nótaí: Is druga siRNA é Leqvio a dhíríonn ar PCSK9 mRNA.Is é seo an chéad teiripe siRNA ar domhan chun colaistéaról a ísliú (LDL-C).Déantar é a riaradh trí instealladh subcutaneous.Laghdaíonn an druga leibhéal próitéin PCSK9 trí chur isteach RNA, rud a laghdaíonn leibhéal LDL-C.Léiríonn sonraí cliniciúla gur féidir le Leqvio LDL-C a laghdú thart ar 50% d’othair nach féidir leo leibhéil LDL-C a laghdú go dtí an spriocleibhéal tar éis cóireála leis an dáileog uasta de statins.
(13)Oscaill
Cuideachta: Arna fhorbairt ag Alnylam Pharmaceuticals.
Am chun an mhargaidh: Formheasta ag an Aontas Eorpach le haghaidh margaíochta i mí na Samhna 2020.
Tásca: Le haghaidh cóireáil hyperoxaluria bunscoile cineál 1 (PH1).
Nótaí: Is druga siRNA é Oxlumo a dhíríonn ar hydroxyacid oxidase 1 (HAO1) mRNA, agus is é an modh riaracháin instealladh subcutaneous.Forbraíodh an druga ag baint úsáide as an cheimic chobhsaithe fheabhsaithe is déanaí ó Alnylam, teicneolaíocht comhchuingeach ESC-GalNAc, a chuireann ar chumas siRNA a riartar go subcutaneously le níos mó marthanachta agus potency.Déanann an druga díghrádú nó bac ar hydroxyacid oxidase 1 (HAO1) mRNA, laghdaítear leibhéal glycolate oxidase san ae, agus ansin ídíonn sé an tsubstráit atá ag teastáil le haghaidh táirgeadh oxalate, laghdaítear táirgeadh oxalate chun dul chun cinn an ghalair a rialú in othair agus feabhas a chur ar na hairíonna galair.
(14) Viltepso
Cuideachta: Arna fhorbairt ag NS Pharma, fochuideachta de chuid Nippon Shinyaku.
Am chun an mhargaidh: Faofa ag an FDA le haghaidh margaíochta i mí Lúnasa 2020.
Tásca: Chun diostróife mhatánach Duchenne (DMD) a chóireáil le exon 53 gan bacadh le sóchán géine sa ghéin DMD.
Nótaí: Is druga antisense oligonucleotide é Viltepso a fhéadann ceangal a dhéanamh le seasamh exon 53 den réamh-mRNA den ghéine DMD, rud a fhágann go ndéanfar cuid de exon 53 a dhíbirt tar éis mRNA aibí a fhoirmiú, rud a cheartaíonn go páirteach an fráma léitheoireachta mRNA Cabhraíonn an bosca le hothair roinnt foirmeacha feidhmiúla de diostróifín a shintéisiú, rud a chuireann feabhas ar na hairíonna de na gnáthphróitéiní atá níos giorra.
(15) Amondys 45
Cuideachta: Arna fhorbairt ag Sarepta Therapeutics.
Am chun an mhargaidh: Faofa ag an FDA le haghaidh margaíochta i mí Feabhra 2021.
Tásca: Chun diostróife mhatánach Duchenne (DMD) a chóireáil le exon 45 gan bacadh le sóchán géine sa ghéin DMD.
Nótaí: Is druga oligonucleotide antisense é Amondys 45, is féidir leis an oligonucleotide antisense ceangal a dhéanamh le seasamh exon 45 den réamh-mRNA de ghéine DMD, rud a fhágann go gcuirtear bac ar chuid exon 45 tar éis foirmiú MRNA aibíochta Excision, rud a cheartú go páirteach ar an mRNA léamh frámaí, ag cabhrú le hothair a shintéisiú foirmeacha léamh gnáth, ag cabhrú othar a shintéisiú foirmeacha níos giorra ná an léamh próitéine. s comharthaí.
(16) Amvutra (vutrisiran)
Cuideachta: Arna fhorbairt ag Alnylam Pharmaceuticals.
Am chun an mhargaidh: Faofa ag an FDA le haghaidh margaíochta i mí an Mheithimh 2022.
Tásca: Chun cóireáil a dhéanamh ar amyloidosis transthyretin hereditary le polyneuropathy (hATTR-PN) i ndaoine fásta.
Nótaí: Is druga siRNA é Amvuttra (Vutrisiran) a dhíríonn ar mRNA trasthyretin (ATTR), a riartar trí instealladh subcutaneous.Tá Vutrisiran bunaithe ar dhearadh ardán seachadta comhchuingeach GalNAc Ceimic Cobhsaíochta Feabhsaithe Alnylam (ESC)-GalNAc le cumas méadaithe agus cobhsaíocht meitibileach.Tá ceadú na teiripe bunaithe ar shonraí 9-mí a staidéar cliniciúil Chéim III (HELIOS-A), agus léiríonn na torthaí foriomlána gur fheabhsaigh an teiripe na hairíonna de hATTR-PN, agus go ndearnadh níos mó ná 50% de riocht na n-othar a aisiompú nó a stopadh ó dhul in olcas.
4. Drugaí géinteiripe eile
(1) Rexin-G
Cuideachta: Arna fhorbairt ag Epeius Biotech.
Am chun an mhargaidh: In 2005, cheadaigh an Riarachán Bia agus Drugaí Philippine (BFAD) é le haghaidh margaíochta.
Tásca: Chun cóireáil a dhéanamh ar ardailsí atá frithsheasmhach in aghaidh ceimiteiripe.
Nótaí: Is instealladh nanacháithníní géine-luchtaithe é Rexin-G.Tugann sé géine mutant cyclin G1 isteach sna spriocchealla trí veicteoir retroviral chun siadaí soladacha a mharú go sonrach.Is é an modh riaracháin insileadh infhéitheach.Mar dhruga meall-dhírithe a lorgaíonn go gníomhach agus a scriosann cealla ailse méadastatacha, tá éifeacht leigheasach áirithe aige ar othair ar theip orthu ar dhrugaí ailse eile, lena n-áirítear bitheolaíoch spriocdhírithe.
(2) Neovasculgen
Cuideachta: Arna fhorbairt ag institiúid gascheall daonna.
Am liostála: Faomhadh é lena liostú sa Rúis an 7 Nollaig, 2011, agus ansin seoladh é san Úcráin in 2013.
Tásca: Le haghaidh cóireáil galair artaireach soithíoch forimeallach, lena n-áirítear ischemia géar géaga.
Nótaí: Is géinteiripe é Neovasculgen atá bunaithe ar plasmid DNA.Déantar géine fachtóir fáis endothelial soithíoch (VEGF) 165 a thógáil ar an gcnámh droma plasmid agus a insileadh isteach in othair.
(3) Collategene
Cuideachta: Comhfhorbartha ag Ollscoil Osaka agus cuideachtaí caipitil fiontair.
Am chun an mhargaidh: Faofa ag Aireacht Sláinte, Saothair agus Leasa na Seapáine i mí Lúnasa 2019.
Tásca: Cóireáil ischemia foirceann íochtair ríthábhachtach.
Nótaí: Is géinteiripe plasmid-bhunaithe é Collategene, an chéad druga géinteiripe baile a tháirg AnGes, cuideachta géinteiripe sa tSeapáin.Is é príomh-chomhpháirt an druga seo ná plasmid naked ina bhfuil seicheamh géine fachtóir fáis heipitocyte daonna (HGF).Má dhéantar an druga a instealladh isteach i matáin na géaga níos ísle, cuirfidh an HGF sainráite chun cinn foirmiú soithigh fola nua timpeall na soithigh fola occluded.Dheimhnigh trialacha cliniciúla a éifeacht ar ulcers a fheabhsú.
Conas is féidir le Foregene cabhrú le forbairt géinteiripe?
Cabhraímid leis an am scagtha a shábháil i scagthástáil ar scála mór, ag céim luath forbartha drugaí siRNA.
Tuilleadh sonraí tabhair cuairt ar:
https://www.foreivd.com/cell-direct-rt-qpcr-kit-direct-rt-qpcr-series/
Am postála: Dec-27-2022